A. PERKEMBANGAN TEORI ATOM
Perkembangan teori atom yang berawal dari konsep yang
dikemukakan oleh Democritus yang mendefinisikan atom berasal dari bahasa
Yunani, atomos (a = tidak, tomos = dibagi-bagi), yang artinya suatu zat yang
tidak bisa dibagi lagi. Tetapi, pendapat Democritus tidak didasarkan pada
eksperimen sehingga kurang kuat dan tidak bisa menjelaskan sifat kimia suatu
materi.
Lalu berkembanglah teori atom John Dalton sampai teori
atom modern yang dikemukakan oleh Heisenberg dan Schrodinger. Teori atom modern
inilah yang masih dipakai sampai saat ini. Bagaimanakah perkembangan teori atom
dari masa ke masa? Ulasan dibawah akan menjelaskan perkembangan teori atom dari
bola pejal sampai ke teori atom modern.
Teori Atom John Dalton
Tokoh dari perkembangan teori atom yang pertama adalah
John Dalton. Pada tahun 1803, John Dalton mengemukakan pendapatnaya tentang
atom. Teori atom yang dikemukakan Dalton didasarkan pada dua hukum, yaitu
1.
Hukum
Kekekalan Massa (Hukum Lavoisier)
Massa total zat-zat sebelum reaksi akan selalu sama
dengan massa total zat-zat hasil reaksi.
2.
Hukum
susunan tetap (Hukum Prouts)
Perbandingan massa unsur-unsur dalam suatu senyawa selalu tetap.
Jika diilustrasikan
dalam bentuk gambar, atom yang dikemukakan oleh Dalton berbentuk seperti bola
pejal.
Gambar atom menurut John Dalton
Kesimpulan Teori Atom John Dalton:
1.
Atom merupakan
partikel terkecil dari suatu materi sehingga tidak dapat dibagi lagi menjadi
bagian yang lebih kecil.
2.
Atom tidak dapat
diciptakan atau dimusnahkan.
3.
Atom digambarkan
seperti bola pejal sederhana dengan ukuran sangat kecil.
4.
Penyusun unsur adalah
atom-atom yang sama.
5.
Penusun senyawa
adalah atom-atom yang berbeda sesuai unsur penyusunnya.
6.
Atom-atom bergabung
membentuk senyawa dengan perbandingan bilangan bulat dan sederhana.
Kelebihan
Teori Atom Dalton
Mampu membangkitkan minat terhadap penelitian tentang
model atom berikutnya.
Kelemahan Teori John Dalton
Tidak bisa mejelaskan hubungan antara larutan senyawa
dan daya hantar arus listrik.
Teori Atom J. J. Thomson
Perkembangan teori atom yang kedua dikemukakan oleh J.
J Thomson. Penemuan tabung katode oleh William Crookers membantu J. J. Thomson
dapat menemukan teori atom baru. Melalui tabung katode, J. J Thomson memastikan
bahwa sinar katode merupakan partikel karena dapat memutar baling-baling yang
diletakkan diantara katode dan anode.
Hasil dari percobaan ini membuktikan bahwa sinar
katode merupakan partikel penyusun atom yang bermuatan negatif (selanjutnya
disebut elektron). Secara ringkas, Thomson menyimpulkan bahwa atom adalah bola
padat bermuatan positif dan di dalamnya tersebar elektron yang bermuatan
negatif. Model atom Thomson digambarkan seperti kismis (elektron) yang berada
pada roti (atom).
Gambar
Teori Atom J. J Thomson
Atom merupakan materi yang bermuatan positif dan
didalamya tersebar elektron (partikel bermuatan negatif).
Kelebihan
Menjadi awal penemuan bahwa atom bukan partikel terkecil sehingga memberi jalan
untuk teori-teori selanjutnya.
Kelemahan:
Thomson tidak dapat menjelaskan susunan muatan positif dan negatif dalam bola
atom tersebut.
Teori Atom Rutherford
Teori atom Rutherford muncul berdasarkan eksperimen
hamburan sinar alfa dari uranium. Rutherford bersama dua orang muridnya (Hans
Geigerdan Erners Masreden) melakukan percobaan yang dikenal dengan hamburan
sinar alfa (α).
Partikel alfa adalah partikel yang bermuatan positif dan bergerak lurus dan
berdaya tembus besar, sehingga dapat menembus lembaran tipis kertas.
Awalnya, percobaan tersebut bertujuan menguji pendapat
Thomson mengenai atom berupa bola pejal yang bermuatan negatif. Hasil dari
percobaan Rutherford adalah hampir semua partikel alfa diteruskan. Jika lempeng
emas tersebut dianggap sebagai satu lapisan atom-atom emas, maka didalam atom
emas terdapat partikel yang sangat kecil yang bermuatan positif.
Kemudian Rutherford mengusulkan model atom yang
menyatakan bahwa atom terdiri dari inti atom (bermuatan positif) yang sangat
kecil dan dikelilingi oleh elektron (bermuatan negatif).
Gambar
Teori Atom Rutherford
1.
Atom bukan merupakan
bola pejal.
2.
Atom terdiri dari
inti atom yang sangat kecil dan bermuatan positif.
3.
Inti Atom dikelilingi
oleh elektron yang bermuatan negatif.
4.
Di dalam inti atom
juga terdapat partikel netral yang berfungsi mengikat partikel-partikel positif
agar tidak saling tolak menolak.
Kelebihan
Mampu mengemukankan ide mengenai inti atom untuk pertama kalinya.
Kelemahan:
Tidak dapat menjelaskan mengapa elektron tidak jatuh ke dalam inti atom
(kestabilan atom) dan spektrum atom hidrogen yang merupakan spektrum garis.
Elektron yang mengelilingi inti atom mengeluarkan energi sehingga ada pasti
saat elektron dapat jatuh ke inti atom.
Teori Atom Bohr
Perkembangan teori atom terus berlanjut pada tahun
1913, Niels Bohr mengembagkan teori atom Rutherford menggunakan percobaan
spektrum hidrogen. Percobaan ini berhasil memberikan gambaran keadaan elektron
dalam menempati daerah disekitar inti atom. Penjelasan Bohr tentang atom
hidrogen melibatkan gabungan antara teori klasik dari Rutherford dan teori
kuantum dari Planck.
Empat postulat hasil percobaan Niels Bohr
1.
Hanya ada seperangkat
orbit tertentu yang diperbolehkan bagi satu elektron dalam atom hidrogen. Orbit
ini dikenal sebagai keadaan gerak stasioner elektron dan merupakan lintasan
melingkar disekeliling inti.
2.
Elektron tidak
memancarkan atau menyerap energi selama elektron berada dalam lintasan
stasioner, sehingga energinya tetap.
3.
Elektron hanya dapat
berpindah dari satu lintasan stasioner ke lintasan stasioner lain.
4.
Lintasan stasioner
yang dibolehkan memilki besaran dengan sifat-sifat tertentu, terutama sifat
yang disebut momentum sudut.
Gambar
Teori Atom Bohr
Kesimpulan Teori Atom Bohr
Atom terdiri atas inti atom yang bermuatan positi dan
elektron-elektron yang mengelilingi inti atom pada lintasan-lintasan tertentu.
Litasan-lintasan tersebut disebut kulit elektron atau tingkat energi. Tingkat
energi paling rendah terdapat pada kulit elektron yang terletak paling dalam.
Sedangkan tingkat energi paling besar terletak pada kulit elektron paling luar.
Semakin jauh dari inti atom (semakin besar nomor kulitnya) maka tingkat
energinya akan semakin tinggi.
Kelebihan
Dapat menjelaskan mengapa elektron tidak jatuh ke inti atom dan spektrum atom
hidrogen.
Kelemahan
Model atom ini tidak bisa menjelaskan spektrum warna dari atom berelektron
banyak.
Teori Atom Modern
Teori Atom modern dikenal juga dengan teori atom
mekanika kuantum. Teori mekanika kuantum dikemukakakn oleh beberapa tokoh
dimana teori satu sama lain saling berhubungan. Tokoh tersebut yaitu:
1.
Louis de Broglie
De
broglie mengemukakan bahwa materi (elektron) memiliki dualisme sifat sebagai
partikel dan gelombang. Sifat elektron sebagai gelombang membuat posisi
elektron tidak bisa dipastikan karena gerakan elektron seperti gelombang yaitu
gerak yang acak.
2.
Werner Heisenberg
Heisenberg
mengemukakan asas ketidakpastian posisi elektron karena menghubungkan dengan
pendapat de Broglie bahwa elektron bergerak acak seperti gelombang.
3.
Erwin Schrodinger
Erwin
Schrodinger melengkapi teori mekanika kuantum melalui suatu persamaan untuk
mendapatkan fungsi gelombang. Fungsi gelombang tersebut digunakan untuk
menggambarkan batas kemungkinan ditemukannya elektron dalam tiga dimensi.
Schrodinger juga merumuskan bentuk dan tingkat energi orbital. Orbital
merupakan daerah di sekitar inti dengan kemungkinan terbesar ditemukan elektron.
Sehingga posisi elektron tidak dapat ditentukan dengan pasti.
Gambar
Model Atom Modern
Kesimpulan Model Atom Mekanika Gelombang:
Elektron-elektron yang mengelilingi inti atom memiliki
tingkat energi tertentu tetapi keberadaannya tidak dapat dipastikan. Posisi
elektron dapat ditemukan padea orbital yaitu daerah kebolehjadian paling besar
untuk menemukan elektron. Elektron menempati orbital yang dinyatakan dalam
bilangan kuantum.
Gerakan elektron memiliki sifat gelombang. Gerak
tersebut mengikuti penyelesaian kuadrat fungsi gelombang yang disebut orbital.
B. STRUKTUR ATOM
Penemuan
Elektron
J.J Thomson menemukan elektron. Thomson melakukan
percobaan Sinar Katode.
C =
katode
A =
anode
E =
lempeng kondensor bermuatan listrik
F =
layar yang dapat berpendar (berfluoresensi)
Hasil
percobaan J.J. Thomson menunjukkan bahwa sinar katode dapat dibelokkan ke arah
kutub positif medan listrik. Hal ini membuktikan terdapat partikel bermuatan
negatif dalam suatu atom.
Sifat – sifat yang
ada di Sinar katode:
·
Merambat tegak lurus dari permukaan katode
menuju anode
·
Merupakan radiasi partikel, terbukti bisa
memutar kincir
·
Bermuatan listrik negatif jadi dibelokkan ke
kutub positif
·
Bisa memendarkan berbagai jenis zat, termasuk
gelas
Muatan elektron ini ditemukan
sama Robert Milikan lewat
percobaan tetesan halus minyak seperti gambar berikut.
Minyak
disemprotkan ke dalam tabung yang bermuatan listrik. Akibat gaya tarik
gravitasi akan mengendapkan tetesan minyak yang turun. Apabila tetesan minyak
diberi muatan negatif maka akan tertarik ke kutub positif medan listrik. Dari
hasil percobaan Milikan dan Thomson diperoleh muatan elektron –1 dan massa
elektron 0, sehingga elektron dapat dilambangkan (0-1e).
Penemuan Proton
Eungene Goldstein menemukan
Proton dengan melakukan percobaan sinar katode yang udah dimodifikasi, yaitu
memberi lubang (saluran) di tengah Katode.
Sifat – sifat Sinar Anode (sinar terusan):
- Merupakan radiasi partikel (bisa memutar kincir)
- Dalam medan listrik atau magnet dibelokkan ke kutub negatif, jadi merupakan radiasi bermuatan positif
- Partikel sinar terusan tergantung pada jenis gas dalam tabung
Penemuan Neutron
James Chadwick menemukan
Neutron melakukan percobaan dengan menembaki atom Berilium dengan sinar alfa.
Neutron gak bermuatan.
Penemuan Inti Atom
Ernest Rutherford dengan 2
muridnya yaitu Hans Geiger dan Ernest Marsden dengan nama Eksperimen penghamburan sinar alpha.
Inti atom tersusun atas proton
dan neutron. Proton dan
neutron disebut yaitu nukleon.
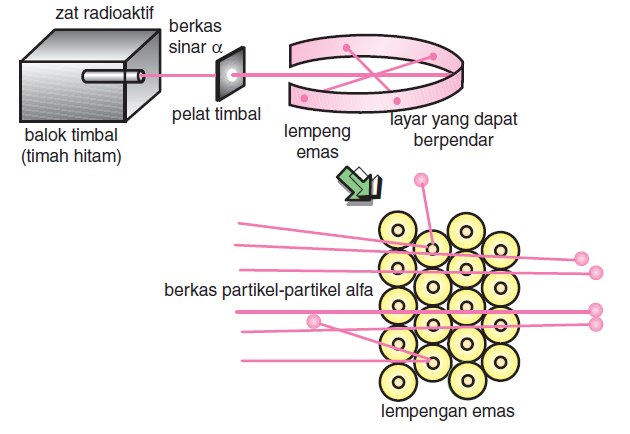
Hasil percobaan ini
membuat Rutherford menyatakan hipotesisnya bahwa atom tersusun dari inti atom
yang bermuatan positif dan dikelilingi elektron yang bermuatan negatif,
sehingga atom bersifat netral. Massa inti atom tidak seimbang dengan massa
proton yang ada dalam inti atom, sehingga dapat diprediksi bahwa ada partikel
lain dalam inti atom.
Tabel Muatan dan Massa elektron,
proton dan neutron
|
Partikel |
Lambang |
Penemu |
Massa |
Muatan |
Coloumb |
|
Elektron
|
e p n |
J.J Thomson
|
9,109 x
10-31 1,673 x
10-27 1,675 x
10-27 |
-1 +1 0 |
1,6 x 10-19 1,6
x 10-19 0 |
Nomor
Atom (Z)
Nomor atom suatu unsur sama dengan jumlah
proton. Buat atom netral, jumlah proton = jumlah elektron.
No. Atom = Jumlah proton = Jumlah elektron
Contohnya: Atom Oksigen bernomor atom 8 jadi
memiliki 8 proton dan 8 elektron.
Nomor
Massa (A)
Nomor massa yaitu jumlah nukleon (proton dan
neutron) yang ada di dalam inti atom.
No. Massa = Jumlah proton + Jumlah neutron
Contohnya: Atom natrium terdiri atas 11
proton dan 12 neutron, berarti nomor massa atom natrium = 11 +
12 = 23
Lambang
Unsur (X)
Susunan suatu unsur netral bisa dinyatakan
dengan lambang dibawah ini:
Dimana :
X = lambang unsur/notasi unsur
Z = nomor atom atau jumlah proton dalam
inti (p) atau jumlah elektron yang mengelilingi inti
A= nomor massa atau jumlah proton +
jumlah neutron (n)
n = neutron (n = A – Z)
Contoh:
Jumlah proton: 6
Jumlah elektron: 6
Jumlah neutron: 12 – 6 = 6
Isotop,
isobar, isoton
1. Isotop
Isotop yaitu atom yang memiliki nomor atom (jumlah proton) sama,
tetapi nomor massanya berbeda. Contohnya:
|
137N |
147N |
157N |
|
p = 7 |
P = 7 |
p = 7 |
|
e = 7 |
e = 7 |
e = 7 |
|
n = 6 |
n = 7 |
n = 8 |
Contoh lain yang merupakan isotop
|
Unsur |
Isotop |
|
Hidrogen |
11H, 12H, 13H |
|
Helium |
23He, 24He, |
|
Karbon |
612C, 613C, 614C |
|
Nitrogen |
714N, 715H |
|
Oksigen |
816O, 817O, 818O |
2. Isobar
Isobar yaitu atom-atom yang berbeda namun memiliki jumlah nomor massa yang
sama. Contohnya:
136C dan 137N
Nomor massa C = 13
Nomor massa N = 13
Contoh lain yang
merupakan isobar
|
Unsur |
Isobar |
|
Hidrogen dan Helium |
13H dan 23He |
|
Karbon dan Nitrogen |
614C dan 714N |
|
Natrium dan Magnesium |
1124Na dan 1224Mg |
3. Isoton
Isoton yaitu atom-atom yang berbeda namun memiliki jumlah neutron
yang sama. Contohnya:
3115O dan 3216N
Jumlah neutron
O = 31-15 = 16
Jumlah neutron N = 31-16 = 16
Contoh lain yang
merupakan isoton
|
Unsur |
Isoton |
Jumlah neutron |
|
Hidrogen dan Helium |
13H dan 24He |
2 |
|
Karbon dan Nitrogen |
613C dan 714N |
7 |
|
Natrium dan Magnesium |
1123Na dan 1224Mg |
12 |
4. Isoelektron
Isoelektron merupakan atom-atom yang mempunyai jumlah elektron sama
setelah melepas atau menangkap elektron. Contohnya:
|
2311Na+ |
199F- |
|
p = 11 |
p = 9 |
|
e = 11 – 1 = 10 |
e = 9 + 1 = 10 |
|
n = 23 – 11 = 12 |
n = 19 – 9 = 10 |
Jumlah elektron Na awalmula adalah 11 kemudian Na melepas satu elektron
(tanda +) yang mengakibatkan jumlah elektron Na berkurang dari 11 menjadi 10.
Jumlah elektron F awalmula adalah 9 kemudian F menangkap satu elektron
(tanda -) yang mengakibatkan jumlah elektron F bertambah dari 9 menjadi 10.
Sumber
https://idschool.net/sma/perkembangan-teori-atom/
https://materikimia.com/isotop-isoton-isobar-dan-isoelektron/










Komentar
Posting Komentar